Diagrama de temas
-
-
Foro
-
-
-

 Colocándose
cuidadosamente una pequeña aguja de acero sobre la superficie
del agua contenida en un recipiente, se observa que puede
permanecer sobre la película superficial sin sumergirse en el
líquido, a pesar de ser mucho más densa que el agua. Se debe
considerar que la superficie se comporta como una membrana
elástica y al ser deformada por el peso de la aguja, es capaz
de sostenerla.
Colocándose
cuidadosamente una pequeña aguja de acero sobre la superficie
del agua contenida en un recipiente, se observa que puede
permanecer sobre la película superficial sin sumergirse en el
líquido, a pesar de ser mucho más densa que el agua. Se debe
considerar que la superficie se comporta como una membrana
elástica y al ser deformada por el peso de la aguja, es capaz
de sostenerla.

Por esta misma razón, pequeños insectos, más densos que el agua pueden moverse sobre la superficie de aguas en reposo.


Consideremos un líquido en equilibrio en un recipiente. Una molécula, situada en el interior del líquido (posición A), es atraída en todas direcciones por las moléculas contiguas y, por eso, la resultante de las fuerzas que actúan sobre ella es prácticamente nula.
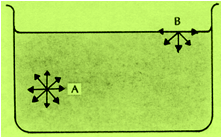 Mientras que en una
molécula situada cerca de la superficie del líquido (posición
B), actúan fuerzas
ejercidas por
moléculas del mismo líquido, como lo muestra la figura y
fuerzas menores, ejercidas por las moléculas del aire
(y del vapor del líquido). Entonces, es
fácil percibir que sobre una molécula cercana a la superficie, habrá una fuerza resultante dirigida hacia abajo,
es decir, hacia el interior del líquido.
Mientras que en una
molécula situada cerca de la superficie del líquido (posición
B), actúan fuerzas
ejercidas por
moléculas del mismo líquido, como lo muestra la figura y
fuerzas menores, ejercidas por las moléculas del aire
(y del vapor del líquido). Entonces, es
fácil percibir que sobre una molécula cercana a la superficie, habrá una fuerza resultante dirigida hacia abajo,
es decir, hacia el interior del líquido.
En virtud de esto, la superficie libre del líquido actúa como una película elástica que resiste tanto una compresión como una distensión. Como se necesita realizar un trabajo para mover una molécula del interior hacia la superficie, en contra de dicha fuerza de cohesión neta, las moléculas superficiales tienen más cantidad de energía mecánica que las moléculas del interior del líquido. La superficie se comporta como una capa especial del fluido con propiedades elásticas debido a las fuerzas de cohesión entre las moléculas de la superficie.
Es decir, en un fluido cada molécula interacciona con las que le rodean. El radio de acción de las fuerzas moleculares es relativamente pequeño, abarca a las moléculas vecinas más cercanas.
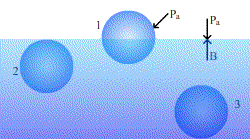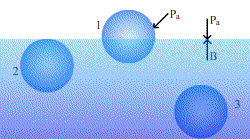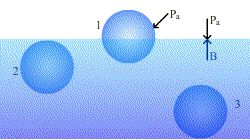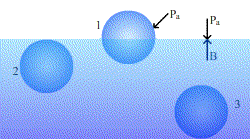
Al analizar la resultante de las fuerzas de interacción sobre una molécula que se encuentra en:
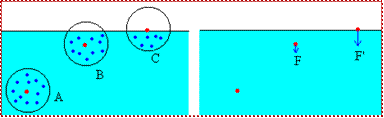
A, el interior del líquido
B, en las proximidades de la superficie
C, en la superficie
Consideremos una molécula (en color rojo) en el seno de un líquido en equilibrio, alejada de la superficie libre tal como la A. Por simetría, la resultante de todas las fuerzas atractivas procedentes de las moléculas (en color azul) que la rodean, será nula.
En cambio, si la molécula se encuentra en B, por existir en valor medio menos moléculas arriba que abajo, la molécula en cuestión estará sometida a una fuerza resultante dirigida hacia el interior del líquido.
Si la molécula se encuentra en C, la resultante de las fuerzas de interacción es mayor que en el caso B.
Las fuerzas de interacción, hacen que las moléculas situadas en las proximidades de la superficie libre de un fluido experimenten una fuerza dirigida hacia el interior del líquido.
Como todo sistema mecánico tiende a adoptar espontáneamente el estado de más baja energía potencial, se comprende que los líquidos tengan tendencia a presentar al exterior la superficie más pequeña posible.
Desde el punto de vista elástico, la tensión superficial es una fuerza de estiramiento, esto es, la fuerza elástica transversal por unidad de longitud de la capa superficial del líquido.
La unidad física de la tensión superficial en el S.I. son N/m.
La superficie de un líquido en reposo, se comporta como una membrana que se alarga bajo tensión. Por ejemplo, una gota de agua en el extremo de un grifo que gotea adquiere una forma casi esférica, como si fuera un pequeño globo lleno de agua.
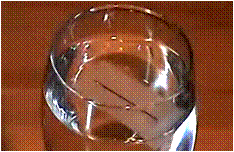 Una aguja de acero
puede flotar sobre la superficie del agua, aun siendo más densa
que el agua. La superficie del líquido actúa como si estuviese
bajo tensión, siendo esta paralela a la superficie, surgiendo
este fenómeno de las fuerzas de cohesión entre las moléculas
del líquido. A este fenómeno (o a su cantidad) se lo denomina
Tensión Superficial γ, que se define como la fuerza por unidad
de longitud que actúa perpendicular a cualquier línea o corte
en la superficie de un líquido.
Una aguja de acero
puede flotar sobre la superficie del agua, aun siendo más densa
que el agua. La superficie del líquido actúa como si estuviese
bajo tensión, siendo esta paralela a la superficie, surgiendo
este fenómeno de las fuerzas de cohesión entre las moléculas
del líquido. A este fenómeno (o a su cantidad) se lo denomina
Tensión Superficial γ, que se define como la fuerza por unidad
de longitud que actúa perpendicular a cualquier línea o corte
en la superficie de un líquido.
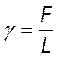
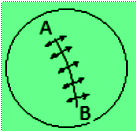 En la figura, se
representa una línea imaginaria de longitud AB, trazada sobre
la superficie de un líquido. Las moléculas situadas en la línea
están accionadas por fuerzas perpendiculares a la línea, del
mismo modo que la membrana tensa de un tambor.
En la figura, se
representa una línea imaginaria de longitud AB, trazada sobre
la superficie de un líquido. Las moléculas situadas en la línea
están accionadas por fuerzas perpendiculares a la línea, del
mismo modo que la membrana tensa de un tambor.
Para comprenderlo, consideremos el sencillo dispositivo de la figura que se utiliza para determinar la Tensión Superficial γ y que consiste en un marco
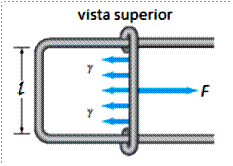
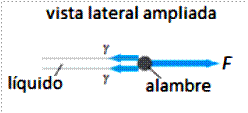
metálico en forma de U y con una parte móvil, que encierra una delgada película de líquido. A medida que este último se va desplazando (a la derecha), la fuerza crece hasta un valor máximo, debido a que la fuerza producida por la película es paralela a ella. Nótese que al correr la parte móvil, a cada lado del alambre se forma una película, por lo tanto la longitud (la longitud de la película tensa es dos veces la del alambre), entonces:
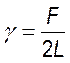
Los jabones y los detergentes tienen el efecto de disminuir la tensión superficial del agua.
Esta propiedad es deseable para lavar y limpiar ya que la alta tensión superficial del agua impide que esta penetre en las fibras del material y en los pequeños intersticios. Las sustancias que reducen la tensión superficial de un líquido se llaman surfacantes.
La tensión superficial también desempeña un papel importante en el fenómeno llamado capilaridad.
¿Cómo se mide la tensión superficial?
Para medir la tensión superficial de un líquido se puede usar un anillo de radio r y extraerlo lentamente, tirando con un dinamómetro, hasta vencer la tensión de la superficie.
Recordemos que la tensión superficial se calcula utilizando la relación:γ=F/L. Si consideramos que la longitud del anillo es 2πr y que la superficie que se estira es doble (por el interior y exterior del anillo), tendremos la siguiente expresión:
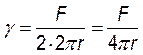
Medida de la tensión superficial de un líquido en forma experimental
El método de Du Nouy es uno de los más conocidos. Se mide la fuerza adicional ΔF que hay que ejercer sobre un anillo de aluminio justo en el momento en el que la lámina de líquido se va a romper. A la derecha el anillo de aluminio suspendido de un dinamómetro.
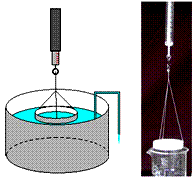
La tensión superficial del líquido se calcula a partir del diámetro 2πr del anillo y del valor de la fuerza ΔF que mide el dinamómetro.
El líquido se coloca en un recipiente, con el anillo inicialmente sumergido. Mediante un tubo que hace de sifón se extrae poco a poco el líquido del recipiente.
En la figura se representa:
1 2 3

- El comienzo del experimento
- Cuando se va formando una lámina de líquido.
- La situación final, cuando la lámina comprende únicamente dos superficies (en esta situación la medida de la fuerza es la correcta) justo antes de romperse.
Si el anillo tiene el borde afilado, el peso del líquido que se ha elevado por encima de la superficie del líquido sin perturbar, es despreciable.
Superficies mínimas: Una superficie sometida a una tensión, tiende a contraerse hasta ocupar el área mínima posible, este es el motivo por el cual una burbuja al interior de un líquido de distinta densidad, tendrá forma esférica.




Consideremos dos recipientes A y B, uno de ellos conteniendo agua y el otro mercurio. Supongamos que sean introducidos en esos líquidos tubos capilares, esto es, tubos de diámetros muy pequeños (el término capilar se usa en este
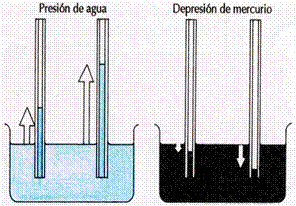 caso porque tiene su
origen en la palabra latina cepillare, que significa "cabello"
y los hilos del cabello, también tienen diámetros muy
pequeños). Observe que en A el agua en el interior de los tubos
capilares alcanza un nivel superior al del agua en el
recipiente y, en B el mercurio se encuentra en el interior de
los tubos, en un nivel inferior. Para explicar esas
observaciones, debemos recordar que el agua moja el vidrio y
así, las fuerzas de adherencia hacen que ella se eleve por
encima del nivel normal. En el caso del mercurio, como las
fuerzas de cohesión son superiores a las de adherencia, el
líquido baja en el tubo capilar. En ambos casos, el fenómeno se
conoce como capilaridad, porque tanto la elevación como el
descenso de nivel sólo se aprecian en tubos delgados, donde el
peso de la columna líquida es mínimo (en estos casos las
fuerzas de adhesión son acciones moleculares de poca
intensidad). Por lo que, mientras más delgado es el tubo, mayor
es la elevación o descenso de nivel del líquido en su
interior.
caso porque tiene su
origen en la palabra latina cepillare, que significa "cabello"
y los hilos del cabello, también tienen diámetros muy
pequeños). Observe que en A el agua en el interior de los tubos
capilares alcanza un nivel superior al del agua en el
recipiente y, en B el mercurio se encuentra en el interior de
los tubos, en un nivel inferior. Para explicar esas
observaciones, debemos recordar que el agua moja el vidrio y
así, las fuerzas de adherencia hacen que ella se eleve por
encima del nivel normal. En el caso del mercurio, como las
fuerzas de cohesión son superiores a las de adherencia, el
líquido baja en el tubo capilar. En ambos casos, el fenómeno se
conoce como capilaridad, porque tanto la elevación como el
descenso de nivel sólo se aprecian en tubos delgados, donde el
peso de la columna líquida es mínimo (en estos casos las
fuerzas de adhesión son acciones moleculares de poca
intensidad). Por lo que, mientras más delgado es el tubo, mayor
es la elevación o descenso de nivel del líquido en su
interior.
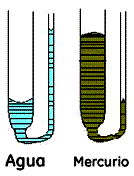
Si observamos el fenómeno “A”, decimos que el líquido “moja” el vidrio. Esto ocurre cuando, por ejemplo, tenemos agua en un recipiente y le introducimos un tubo delgado. Vemos cómo el agua penetra en el interior del tubo y alcanza una altura superior al nivel que tiene el agua en el recipiente. Es como si las partículas de agua “treparan” por las paredes del tubo, “mojándolas”.
Si observamos el fenómeno “B”, decimos que el líquido “no moja” el vidrio. Supongamos que tenemos mercurio en un recipiente y le introducimos un tubo muy fino. El mercurio penetra en el tubo pero su superficie libre no alcanza el nivel del líquido dentro del recipiente. Es como si al mercurio “le costara trepar” por las paredes del tubo.
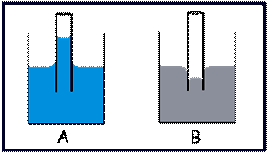 Estos dos fenómenos dependen de las magnitudes relativas
de las fuerzas de cohesión entre las partículas del fluido y
las fuerzas de adhesión de las partículas del fluido a las
paredes del recipiente. En “A” las fuerzas de adhesión son
mayores que las de cohesión y en “B” las fuerzas de cohesión
son mayores que las de adhesión.
Estos dos fenómenos dependen de las magnitudes relativas
de las fuerzas de cohesión entre las partículas del fluido y
las fuerzas de adhesión de las partículas del fluido a las
paredes del recipiente. En “A” las fuerzas de adhesión son
mayores que las de cohesión y en “B” las fuerzas de cohesión
son mayores que las de adhesión.
En varias situaciones, el fenómeno de la capilaridad desempeña un papel importante:
- En una vela, gracias a la capilaridad, la cera derretida sube por el pabilo para alimentar la llama.
- La humedad del suelo sube en una pared en virtud de pequeños y numerosos vasos capilares (porosidad) allí presentes.
- Cuando en el extremo de un trozo de tela (o papel) seco, se introduce en agua, se observa que este líquido alcanza gran parte del tejido no sumergido, porque el líquido se conduce por capilaridad, a través de las pequeñas separaciones entre las fibras del tejido.
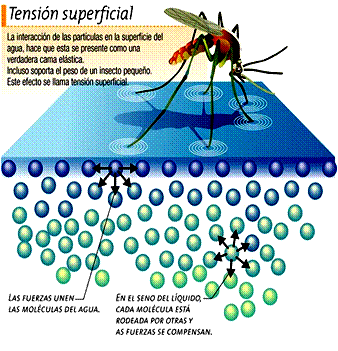 Una molécula bajo la
superficie es atraída por igual en todas direcciones por las
otras moléculas que la rodean. En cambio, una molécula en la
superficie solo es atraída hacia los lados y hacia abajo. Esto
proporciona la tensión superficial suficiente para soportar el
peso del mosquito.
Una molécula bajo la
superficie es atraída por igual en todas direcciones por las
otras moléculas que la rodean. En cambio, una molécula en la
superficie solo es atraída hacia los lados y hacia abajo. Esto
proporciona la tensión superficial suficiente para soportar el
peso del mosquito.
Se puede entender por qué ocurren estos fenómenos analizando la diferencia entre las siguientes fuerzas moleculares:
• Fuerzas de atracción entre las moléculas del propio líquido, que tienden a mantenerlas unidas, denominadas comúnmente fuerzas de cohesión.
• Fuerzas de atracción entre las moléculas del líquido y las del sólido con las que el líquido está en contacto, que tienden a hacer que éste se mantenga adherido al sólido. Se denominan fuerzas de adherencia (o de adhesión).
En el caso del agua con el vidrio, las fuerzas de adherencia son mayores que las de cohesión y, por este motivo, el agua se adhiere al vidrio, mojándolo. En el caso del mercurio con el vidrio, las fuerzas de cohesión entre las moléculas del líquido son mayores que las fuerzas de adherencia ejercida sobre ellas por el vidrio. Por eso, el líquido tiende a tomar la forma esférica y no se adhiere al vidrio (no lo moja). Tenemos esta misma situación en el caso del agua colocada sobre un vidrio engrasado. En este caso, el agua toma la forma de pequeñas gotas y no moja al vidrio.
Entonces se tiene:
 Cuando un líquido entra
en contacto con un sólido, las fuerzas de adhesión (atracción
entre las moléculas del líquido y del sólido), pueden ser
mayores o menores que las fuerzas de cohesión (atracción entre
las moléculas del mismo líquido). En el primer caso, el líquido
moja al sólido (por ejemplo: agua en contacto con vidrio), en
el segundo caso, el líquido no moja al sólido (por ejemplo:
mercurio en contacto con el vidrio).
Cuando un líquido entra
en contacto con un sólido, las fuerzas de adhesión (atracción
entre las moléculas del líquido y del sólido), pueden ser
mayores o menores que las fuerzas de cohesión (atracción entre
las moléculas del mismo líquido). En el primer caso, el líquido
moja al sólido (por ejemplo: agua en contacto con vidrio), en
el segundo caso, el líquido no moja al sólido (por ejemplo:
mercurio en contacto con el vidrio).
Fenómeno de capilaridad con el agua y con el mercurio. Observe que la superficie libre del agua es cóncava y la del mercurio, convexa.
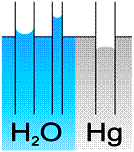
Si colocas un poco de agua sobre la superficie de una placa de vidrio limpia, se esparce sobre el vidrio, adhiriéndose y decimos que el agua "moja" el vidrio. Mientras que si el experimento se repitiera con mercurio, se observaría que se formarían gotas con este líquido sin presentar adherencia al vidrio, es decir, el mercurio no "moja" el vidrio.



-